Sepsis & Autoimmunität
Die Sepsis ist ein komplexes Syndrom, das durch eine fehlregulierte Immunreaktion auf eine Infektion entsteht und zu lebensbedrohlichen Dysfunktionen von Organen führt. Trotz intensiver Forschung über die Sepsis-assoziierten Pathomechanismen sind die Fortschritte in Punkto Prävention, Diagnose und Therapie begrenzt, sodass die Sepsis noch immer mit einer hohen Mortalität und bei Überlebenden mit einer langanhaltenden Morbidität verbunden ist.
Bis heute ist nicht eindeutig geklärt, warum die Immunreaktion nach einer Infektion entgleist und eine Sepsis auslöst. Tatsächlich tritt die Sepsis am häufigsten bei Menschen auf, die an einer chronischen Erkrankung leiden. Prominente Beispiele sind hierbei Krebsleiden, Diabetes und die rheumatoide Arthritis (Abbildung 1).
Abbildung 1: Bis heute ist nicht eindeutig geklärt welche immunologischen Mechanismen mit einer Abwehrreaktion verbunden sind, die zur Widerstandsfähigkeit führen. Im Umkehrschluss ist nicht ausreichend verstanden, unter welchen Bedingungen eine dysregulierte Immunantwort entsteht und damit eine Sepsis auslöst.
Die rheumatoide Arthritis ist eine der prävalentesten Autoimmunerkrankung, bei der hauptsächlich die Gelenke von einer chronischen Entzündung betroffen sind. Auf Grund mangelnder experimenteller Daten ist hierbei nicht verstanden warum Patienten, die an dieser entzündlichen Erkrankung leiden, häufiger komplikationsreiche Infektionsverläufe entwickeln und warum diese mit erhöhter Wahrscheinlichkeit eine Sepsis bedingen.
In unserer Arbeitsgruppe haben wir deshalb ein experimentelles Modell entwickelt, in dem wir die humane Erkrankung mit Hilfe einer Kollagen-induzierten Arthritis (Collagen-induced Arthritis, CIA) in Mäusen mit einer Gruppe A Streptokokkus (GAS-)Infektion kombinierten (Abbildung 2A). Im Vergleich mit Tieren ohne CIA stellten wir fest, dass Mäuse mit der entzündlichen Vorerkrankung einen Zytokinsturm entwickelten und signifikant häufiger lebensbedrohliche Komplikationen, einschließlich des septischen Schocks, entwickelten (Abbildung 2B-C).
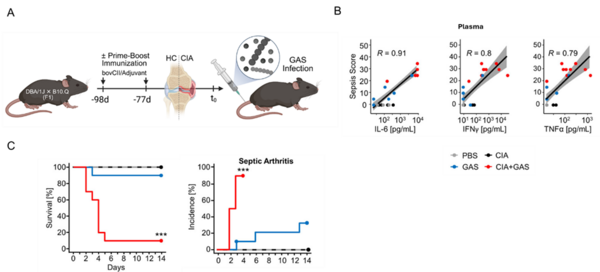
Abbildung 2: Eine autoimmune Arthritis prädisponierte im Mausmodell für die Sepsis. (A) Experimentelles Design. Die Mäuse wurden zweifach mit bovinem Kollagen in Adjuvanz immunisiert, woraufhin Entzündungen an den Gelenken entstanden (CIA). Kontrollmäuse wurden nicht immunisiert (HC). Es wurden die Tiere aus beiden Gruppen intravenös mit Gruppe A Streptokokkus (GAS) infiziert. (B) Die Punktdiagramme visualisieren den linearen Zusammenhang der infektionsassoziierten Krankheitsaktivität (d.h. Sepsis Score) mit der Plasmakonzentration von Interleukin (IL-)6, Interferon (IFN)? und Tumornekrosefaktor (TNF)a. R: Korrelationskoeffizient (C) Die Kaplan-Meier-Kurven stellen den zeitlichen Verlauf der Überlebenswahrscheinlichkeit dar, die unter Verwendung der identifizierten humanen Endpunkte geschätzt wurde (links) und zeigen den Inzidenzverlauf der septischen Arthritis (rechts). ***p < 0,001; Log-rank Test (CIA+GAS vs. GAS).
Nach Analyse der frühen Immunreaktion 24 bzw. 48 Stunden nach Infektion stellten wir in einer Assoziationsstudie fest, dass chronisch entzündete Gelenke und gelenkdrainierende Lymphknoten von CIA Mäusen eine hohe Anzahl aktivierbarer Zellen enthielt, die in Folge der Infektion zu der überschießenden Zytokinproduktion beitrugen (Abbildung 3). Die Lymphadenopathie und synoviale Entzündung sind Hauptmerkmale der rheumatoiden Arthritis und können durch eine geeignete Therapie behandelt werden. Aus diesem Grund schlussfolgerten wir, dass die Induktion einer anhaltenden Remission nicht nur das primäre Ziel der Rheuma-Heilverfahren darstellt, sondern auch maßgeblich dazu beitragen kann, das Sepsis-Risiko von betroffenen Patienten zu reduzieren.
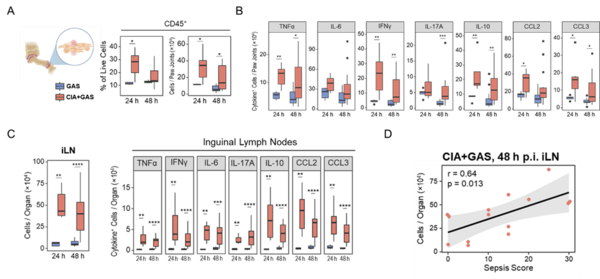
Abbildung 3: Synoviale und nodale Zytokinhyperproduktion in chronisch entzündetem Gewebe bei Mäusen mit autoimmuner Arthritis. Die Boxplots zeigen die chronische Infiltration (A) und erhöhte Frequenz zytokinproduzierender Zellen (B) in den Gelenken von CIA-Mäusen nach Infektion. Weiterhin ist dargestellt, dass Mäuse mit CIA eine erhöhte Zellularität der gelenkdrainierenden inguinalen Lymphknoten (iLN) aufwiesen, was mit einer erhöhten Anzahl von zytokinproduzierenden Zellen auch in diesem Organ einherging (C). Der Dotplot zeigt eine starke Korrelation der iLN-Zellzahl mit dem Sepsis Score (D). *p < 0,05; **p < 0,01; ***p < 0,001; MWU Test.
Dieses Projekt, welches von der DFG (VO 2697/2-1) gefördert wurde, stellt einen Startpunkt bei der Erforschung von grundlegenden Risiko- und Resilienzfaktoren im Zusammenhang mit der Sepsis dar. In Zukunft werden von unserer Arbeitsgruppe weitere Aspekte der Prädisposition für die Sepsis bezüglich einer vorliegenden rheumatischen Grunderkrankung untersucht. Abgesehen vom Erkenntnisgewinn sollen die Folgeprojekte perspektivisch dazu beitragen, die Sepsis schneller zu erkennen und – in Abhängigkeit von der entzündlichen Vorerkrankung – gezielter zu behandeln.
Themen-spezifische Publikationen
- Volzke J, Schultz D, Kordt M, Müller M, Bergmann W, Methling K, Kreikemeyer B, Müller-Hilke B. Inflammatory Joint Disease Is a Risk Factor for Streptococcal Sepsis and Septic Arthritis in Mice. Front Immunol (2020) 11:579475. doi: 10.3389/fimmu.2020.579475
- Volzke J, Müller-Hilke B. Degenerative Joint Damage Is Not a Risk Factor for Streptococcal Sepsis and Septic Arthritis in Mice. (2021) 11:794. doi: 10.3390/life11080794
- Aleith J, Brendel M, Weipert E, Müller M, Schultz D, Müller-Hilke B. Influenza A Virus Exacerbates Group A Streptococcus Infection and Thwarts Anti-Bacterial Inflammatory Responses in Murine Macrophages. Pathogens (2022) 11:1320. doi: 10.3390/pathogens11111320
- Aleith J, Bergmann-Ewert W, Müller-Hilke B. Maximizing Insights, Minimizing Animal Testing: A Framework for Validating Multiparametric Single-Cell Cytokine Analysis Panels. Eur J Immunol (2025) 55: doi: 10.1002/eji.202451193
- Brunsch V, Bergmann-Ewert W, Müller-Hilke B, Aleith J. Interleukin-6 overexpression and elevated granulocyte-to-lymphocyte ratio indicate hepatic stress in experimental group a Streptococcus sepsis. Med Microbiol Immunol (2025) 214:17. doi: 10.1007/s00430-025-00826-2
- Aleith J, Bergmann-Ewert W, Müller-Hilke B. Lymphadenopathy and synovial hyperplasia are associated with sepsis risk in an experimental model of rheumatoid arthritis. Front Immunol (2025) 16: doi: 10.3389/fimmu.2025.1671137
